Ново Нордиск је 5. јула покренуо клиничко испитивање фазе ИИИ ињекције ЦагриСема у Кини, чија је сврха да упореди безбедност и ефикасност ињекције ЦагриСема са семеглутидом код гојазних и гојазних пацијената у Кини.
ЦагриСема ињекција је комбинована терапија дугог дејства коју развија Ново Нордиск, главне компоненте су ГЛП-1 (глукагон-сличан пептид-1) рецептор агонист смеглутид и дугоделујући аналог амилина кагрилинтид.ЦагриСема ињекција се може применити субкутано једном недељно.
Примарни циљ је био да се упореди ЦагриСема (2,4 мг/2,4 мг) са семеглутидом или плацебом једном недељно субкутано.Ново Нордиск је објавио резултате испитивања лека ЦагриСема за лечење дијабетеса стадијума 2, који су доказали да је хипогликемијски ефекат ЦагриСема бољи од семеглутида, а скоро 90% испитаника је постигло циљ ХбА1ц.
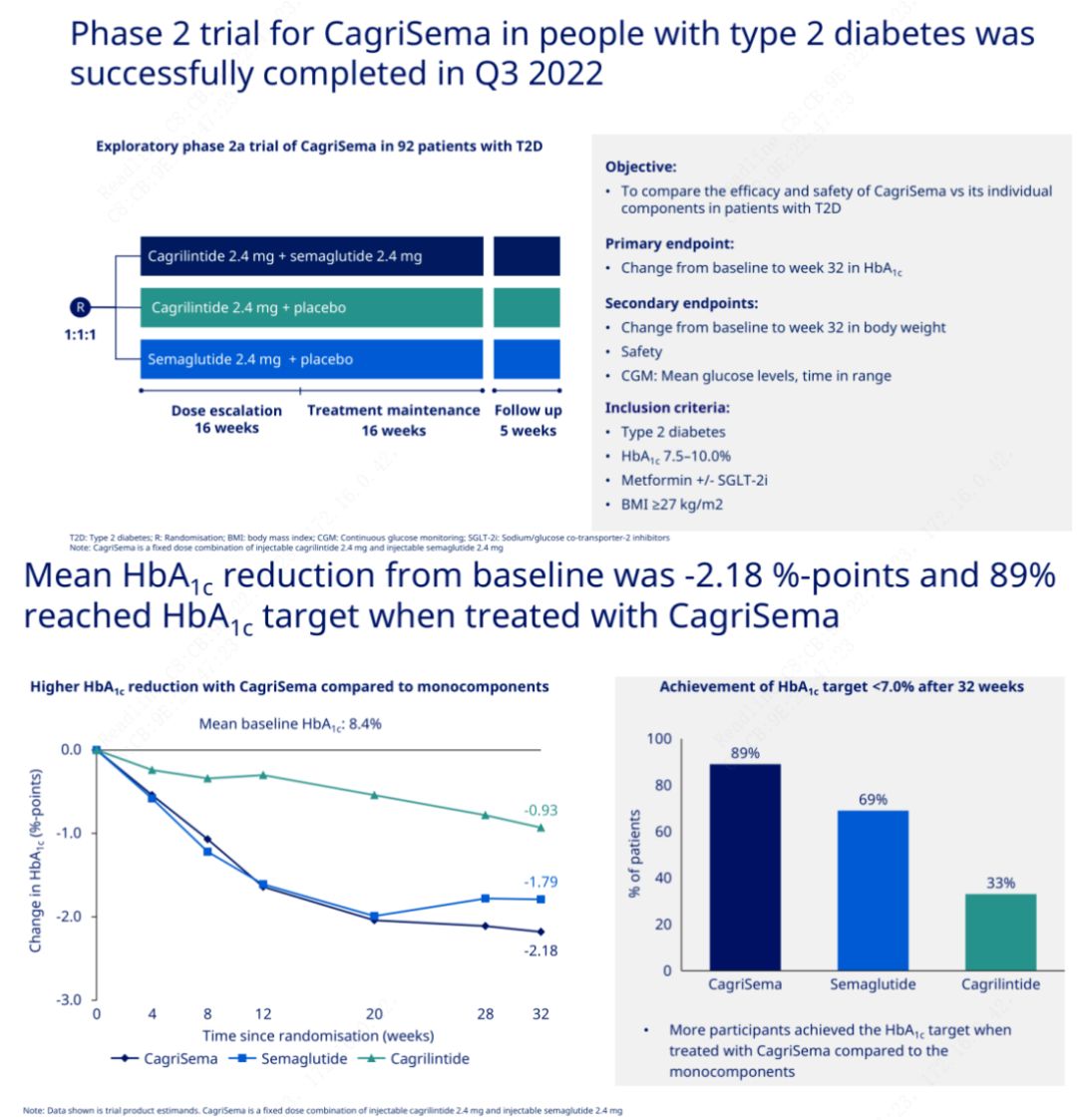
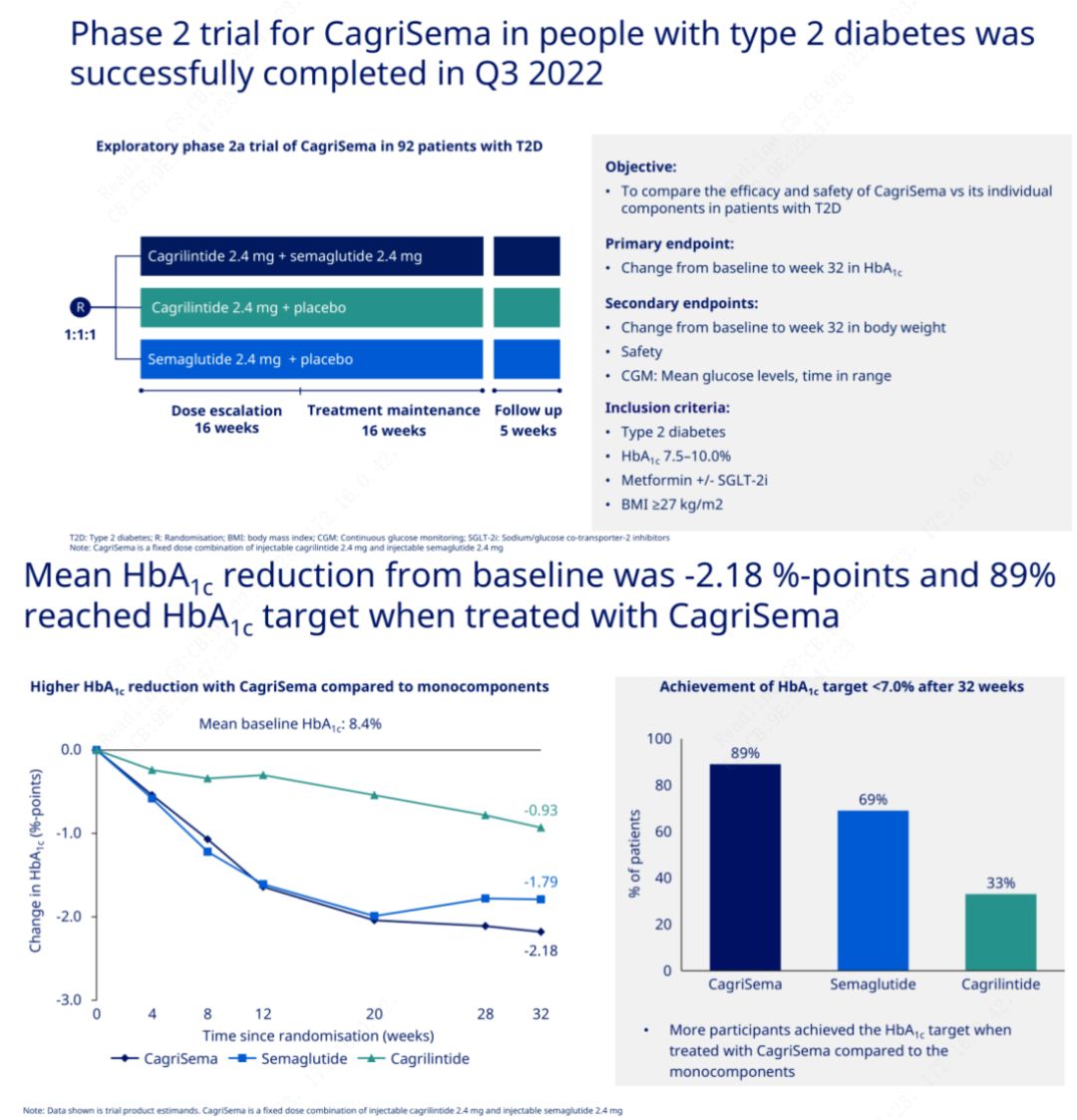
Подаци су показали да је поред значајног хипогликемијског ефекта, у смислу губитка тежине, ЦагриСема ињекција значајно надмашила семеглутид (5,1%) и кагрилинтид (8,1%) са губитком тежине од 15,6%.
Иновативни лек Тирзепатид је први одобрени недељни агонист ГИП/ГЛП-1 рецептора на свету.Комбинује ефекте два инкретина у један молекул који се убризгава једном недељно и представља нову класу третмана за дијабетес типа 2.Тирзепатид је одобрила Америчка управа за храну и лекове (ФДА) у мају 2022. за побољшање контроле гликемије (на бази исхране и вежбања) код одраслих са дијабетесом типа 2 и тренутно је одобрен у Европској унији, Јапану и другим земљама.
Ели Лилли је 5. јула најавио студију фазе ИИИ СУРПАСС-ЦН-МОНО о регистрацији клиничког испитивања лека и платформи за откривање информација за лечење пацијената са дијабетесом типа 2.СУРПАСС-ЦН-МОНО је рандомизована, двоструко слепа, плацебом контролисана студија фазе ИИИ дизајнирана да процени ефикасност и безбедност монотерапије тирзепатидом у поређењу са плацебом код људи са дијабетесом типа 2.Студија је планирала да обухвати 200 пацијената са дијабетесом типа 2 који нису узимали никакве антидијабетичке лекове 90 дана пре посете 1 (осим у одређеним клиничким ситуацијама, као што су акутна болест, хоспитализација или елективна операција, краткорочно (≤14). дана) употреба инсулина).
Очекује се да ће дијабетес типа 2 бити одобрен ове године
Прошлог месеца, резултати студије СУРПАСС-АП-Цомбо објављени су 25. маја у часопису Натуре Медицине.Резултати су показали да је у поређењу са инсулином гларгин, Тирзепатид показао бољи ХбА1ц и смањење телесне тежине у популацији пацијената са дијабетесом типа 2 у азијско-пацифичком региону (углавном Кина): смањење ХбА1ц до 2,49% и смањење тежине до 7,2 кг (9,4%) након 40 недеља лечења, значајно побољшање липида у крви и крвног притиска, и укупна безбедност и подношљивост били су добри.
Клиничко испитивање фазе 3 СУРПАСС-АП-Цомбо је прва студија Тирзепатида која је спроведена углавном на кинеским пацијентима са дијабетесом типа 2, коју је водио професор Ји Линонг из Пекиншке универзитетске народне болнице.СУРПАСС-АП-Цомбо је у складу са резултатима глобалне серије истраживања СУРПАСС, што даље доказује да је патофизиологија дијабетеса код кинеских пацијената у складу са оном код глобалних пацијената, што је основа за истовремено истраживање и развој нових лекова. у Кини и свету, а такође пружа чврсте доказе за пружање могућности кинеским пацијентима да користе најновије лекове за лечење дијабетеса и њихову клиничку примену у Кини што је пре могуће.
Време поста: 18.09.2023

